李兰娟团队:新冠突变影响致病性,体外感染显示270倍差异
来源:观察者网
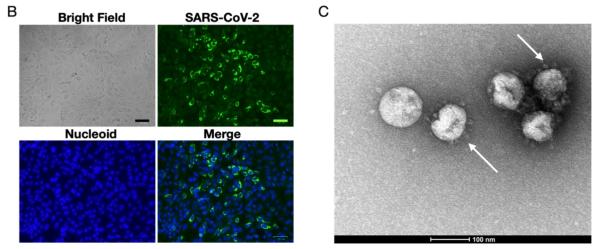
目前关于新冠病毒(SARS-CoV-2)的基因组调查数据表明,病毒存在着大量的单核苷酸变异(SNVs),此前尚无研究表明突变与病毒致病性的功能改变直接相关。
然而,李兰娟院士团队的最新研究提出了直接证据,证明目前发生在新冠病毒基因组中的突变具有影响病毒致病性的功能潜力。李兰娟团队提示:疫苗和药物的开发需要考虑到这些累积突变,尤其是始祖突变的影响,以避免潜在的缺陷。
在最新的一份研究中,来自浙江大学的研究团队报告了11例新冠患者来源的病毒分离株的功能特征,它们都至少有一个突变。重要的是,当感染Vero-E6细胞时,这些病毒分离株在细胞病变效应和病毒载量方面表现出显著差异,差异高达270倍。
当地时间4月19日,浙江大学医学院附属第一医院传染病诊治国家重点实验室、浙江大学生命科学研究院、浙江省胰腺病研究重点实验室的研究团队在医学预印本平台medRxiv在线发表了一篇研究论文“Patient-derived mutations impact pathogenicity of SARS-CoV-2”。该论文通讯作者为中国工程院院士、国家卫健委高级别专家组成员李兰娟教授,浙江大学生命科学研究院研究员蒋超,浙江大学医学院附属第一医院传染病诊治国家重点实验室吴南屏教授和郑敏教授。
目前的研究认为,跨膜刺突糖蛋白(S蛋白)介导病毒进入宿主细胞,S蛋白根据蛋白结构功能又被分为两个功能单位,即S1和S2蛋白亚基。其中S1负责与宿主细胞受体结合,S2负责病毒和细胞膜融合。新冠病毒和SARS-CoV都使用血管紧张素转换酶2(ACE2)进入靶细胞。ACE2在人鼻上皮细胞和肺、精原细胞、间质细胞、支持细胞、胃、十二指肠和直肠上皮细胞中表达。
论文提到,S蛋白的受体结合域(RBD)是β冠状病毒中最具变异性的基因组部分,S蛋白的某些位点可能会受到正向选择。不过,尽管新冠病毒具有大量的变异性,一个关键的问题仍然是:这些突变是否对新冠病毒的致病性有任何真正的功能影响?
研究人员认为,上述问题对理解病毒感染机制至关重要,并指导药物和疫苗的开发战略,为应对疫情大流行下一阶段做准备。为了解决这一问题,研究人员从浙江大学附属第一医院收治的患者中分离出11株新冠病毒毒株。
研究人员在Novaseq 6000平台上对11株病毒分离株进行超深度测序,发现病毒分离株的编码序列分别存在1-5个突变,同样也观察到混合群体(代表病毒准种,Quasi-species)。他们总共鉴定出33个突变(包括在混合群体中观察到的10个突变),根据与GISAID在2020年3月24日提供的1111个基因组序列的比较,其中19个是新的突变。
研究人员还用11株病毒分离株感染了Vero-E6细胞,并定量评估了它们在感染后(P.I.)1、2、4、8、24和48小时的病毒载量,以及在感染后48和72小时的病毒性细胞病理效应(CPE)。
他们的研究结果表明,在感染Vero-E6细胞时,观察到的突变会对病毒载量和细胞病理效应产生直接影响,差异最高达270倍。这一发现表明,研究中观察到的病毒突变,可以显著影响新冠病毒的致病性,而这种突变在全球各地采集的病毒毒株中都可能存在。
总体而言,这项研究提供了直接证据,证明目前发生在新冠病毒基因组中的突变具有影响病毒致病性的功能潜力。研究人员提醒,除了不断积累的基因组测序数据外,还应尽可能在细胞水平上进行病毒监测。最后,与流感类似,药物和疫苗的开发虽然紧迫,但也需要考虑到这些累积突变,尤其是始祖突变的影响,以避免潜在的缺陷。



















